Stal ma dużo zalet, jednak jej wielką wadą jest brak odporności na korozję. Pod wpływem Tlenu (O2) i Wody (H2O) na powierzchni stali tworzy się rdza. Nóż rdzewieje w kieszeni!

Rys. 1 Rdza na stali [2]
Pierwiastkiem który najsilniej wpływa na odporność na korozję stali jest Chrom (Cr). Wraz ze wzrostem jego zawartości (począwszy od 3%) wzrasta znacznie odporność stali na tworzenie się na jej powierzchni rdzy.
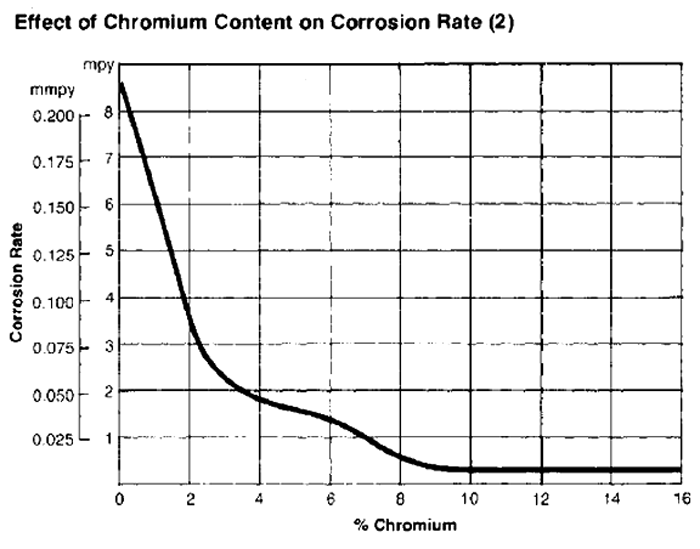
Rys. 2 Wpływ zawartości Chromu na szybkość korozji w stali [2]
Metale szlachetne to takie metale, które słabo korodują w normalnych warunkach (w sumie wcale). Stal z dodatkiem chromu powyżej 12% zachowuje się jak metale szlachetne! Wtedy na powierzchni stali szlachetnej (>12% Chromu) tworzy się cienka, bezbarwna, twarda warstwa Tlenków Chromu chroniąca stal przed korozją. Nazywana jest czasem warstwą pasywną,
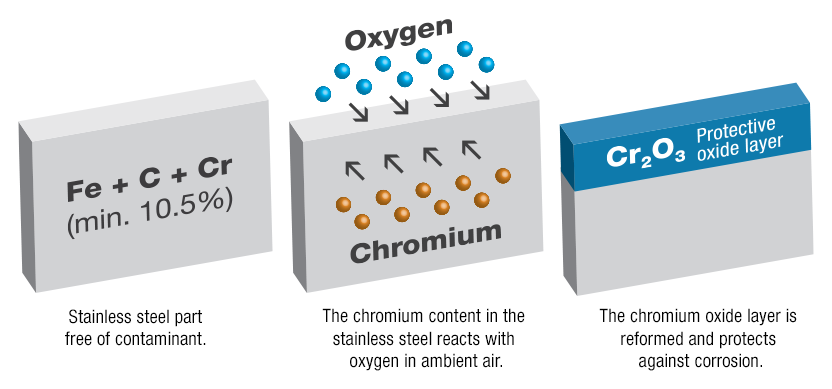
Rys. 3. Tworzenie się warstwy pasywnej na stali szlachetnej [3]
Co ważne warstwa ta tworzy się samoistnie na powierzchni stali, ma też ważną własność: sama się regeneruje po uszkodzeniu mechanicznym!
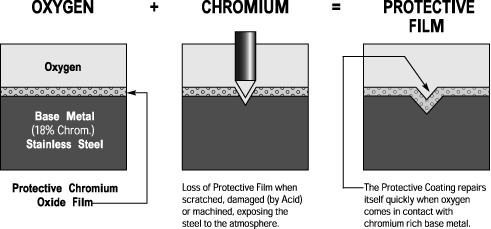
Rys. 4 Regeneracja uszkodzonej warstwy pasywnej [4]
Normy podają, że stal o zawartości 10,5% Chromu jest stalą nierdzewną. Jest to prawdą, ale w stalach konstrukcyjnych, na balustrady czy w architekturze. W stalach narzędziowych nierdzewnych Węgiel (C) zawarty w stali „kradnie” część Chromu, tworząc Węgliki Chromu. I okazuje się, że stal o zawartości np. 11% Chromu, ma tego pierwiastka do ochrony przed korozją tylko 7%, reszta jest „uwięziona” w Węglikach, przykład: stal D2 (AISI). Stal D2 przez to nie jest stalą nierdzewną, mimo, że spełnia definicję! Dlatego w stalach nierdzewnych na noże (o zawartości Węgla do 2%!) zawartość Chromu jest podniesiona do ponad 14%, a przy bardzo dużej zawartości węgla i wysokich wymaganiach antykorozyjnych do ponad 20%.

Rys. 5 Korozja na stali D2, nóż tylko leżał przez pół roku w domu! [5]


Rys. 6 i 7 Korozja na stali D2, nóż był zanurzony przez 2 dni w wodzie lekko posolonej! [6]
Niestety stale nierdzewne nie są idealne, co prawda nie pokrywają się rdzą, jednak występuje w nich inny rodzaj korozji. Podczas obróbki cieplnej, przy kumulacji niekorzystnych czynników stal może zostać uczulona na korozję międzykrystaliczną (Intergranular corrosion). Wtedy na granicach ziarn w stali tworzą się Węgliki Chromu (Cr23C6), które „kradną” Chrom z okolicy, obniżając zawartość tego pierwiastka w swoich okolicach do poniżej 12%. Tworzy się ogniwo galwaniczne, stal zjada sama się w obecności Wody (nawet tej z powietrza)! W wyniku tego w stali pojawia się „trąd” J, wypadają ze stali ziarenka, oddzielone od klingi korozją.
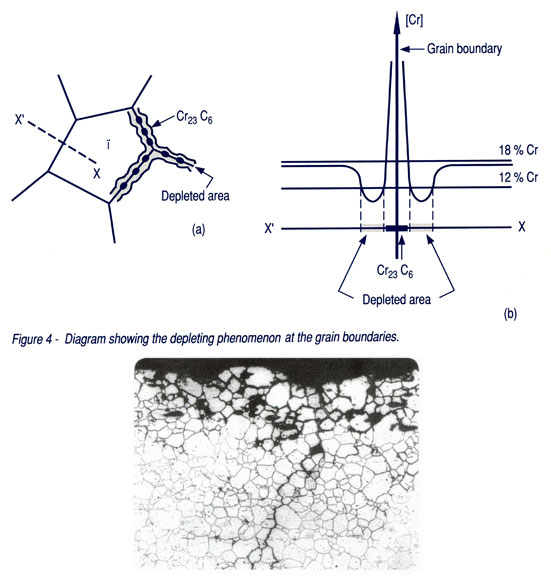
Rys. 8 Korozja międzykrystaliczna, schemat [7]

Rys. 9. Korozja międzykrystaliczna, nóż [8]
Na szczęście zjawisko to jest znane producentom noży w Polsce, wiedzą oni też jak chronić stal przed korozją miedzykrystaliczną.
Są stale na narzędzia, odporne na korozję międzykrystaliczną (nie są stalami nierdzewnymi), korodują, ale bardzo powoli, to stale prawie nierdzewne (semi stainless). Charakteryzują się zawartością Chromu powyżej 5%, korzystnie 7-9%. Pokrywają się z czasem rdzą (bardzo, bardzo, bardzo długo), do tego ta rdza wygląda na nich ładnie, jak patyna.
Literatura
[1] https://mlodytechnik.pl/eksperymenty-i-zadania-szkolne/chemia/5381-korozja-metali
[3] https://www.walter.com/surfox/passivation
[4] http://www.jamesglen.com.au/finishes-and-coatings/
[5] http://knives.pl zdjęcie usera Pitt
[6] http://knives.pl zdjęcia usera Escorpio
[7] http://www.christoforidis.gr/en/intergranular_corrosion.php